Si bien mundialmente ya al coronavirus se lo asimila como un fenómeno ondulante, que cada cierto tiempo presenta una nueva ola, tras bambalinas y de forma más constante, lenta y desapercibida, existe un problema emergente que nos recuerda que la evolución de las especies por selección natural no es solo una teoría.
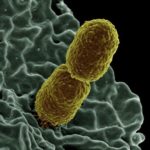
Se trata de un problema global y creciente, las bacterias multirresistentes. En esta ocasión se abordará las estrategias implementadas en laboratorios y los esfuerzos realizados por diferentes institutos para fomentar prácticas destinadas a detener el avance de estos agentes, así como cuestiones que impiden la implementación de estas medidas.
Antesala de la era posantibiótica
Pronósticos ominosos pero también realistas se han hecho sobre la mortalidad de estas bacterias si no se adoptan las medidas adecuadas. De hecho, se habla de una “era posantibiótica” cuando nuestras mejores armas contra las bacterias pierdan eficacia en el tratamiento.
En 2017, la Organización Mundial de la Salud (OMS) publicó una lista de 12 de las principales bacterias multirresistentes peligrosas para el ser humano. Entre estas, son tres las principales: Acinetobacter baumanni, Pseudomonas aeruginosa y las del género Enterobacteriaceae.
La revista Lancet publicó que en 2019 “1,27 millones de personas habían muerto a causa de la inefectividad de los antibióticos” pero que bien podría extenderse esta cifra hasta casi 5 millones, debido al subregistro. Si bien el problema existe de modo global, como se ha dicho, es más acuciante en países en vías de desarrollo, ya que el uso de antibióticos es más laxo y, por tanto, más indiscriminado, pilar fundamental de la resistencia bacteriana.
Es lo que se llama terapia empírica; a determinadas infecciones se las trata con antibióticos sin aún conocer exactamente cuál es el agente que lo provoca y menos aún a qué antibiótico este es sensible. Otro rasgo “folclórico” es la vehemencia con la que los mismos pacientes solicitan los antibióticos, de manera que el médico se siente impelido a prescribirlos incluso cuando no son necesarios.
La primera estrategia implementada poco tiene que ver con infraestructura o insumos costosos y mucho con educación. A modo de ejemplo, en Alemania ya en 2008 se habían fijado metas nacionales bajo el nombre DART (Deutschen Antibiotika Resistenzstrategie).
Aquí se recomienda como pilar de esta lucha el “uso eficiente de antibióticos con la implementación adecuada de las medidas de higiene”. Además, asegura que “la reducción de la resistencia antibiótica solo es posible con la conjugación de la vigilancia sanitaria, la prevención de infecciones, el uso eficiente de antibióticos y el refuerzo continuo en la capacitación del personal médico así como la investigación y el desarrollo”.(1)
Antibióticos de reserva
Otro pilar es una estrategia que promete la salida más rápida a la resistencia, aunque implica seguir jugando el mismo juego, a saber, el uso de nuevos antibióticos contra los cuales no existe tal resistencia. Se han lanzado al mercado ya varios.
Por ejemplo, en 2019 se autorizó el uso de Quofenix, con el nuevo principio activo delafloxacin, de la familia de las quinolonas (un ejemplo conocidísimo es la ciprofloxacina, usada tan comunmente en infecciones urinarias) indicado para “el tratamiento de infecciones bacterianas agudas de la piel y estructuras asociadas” (ABSSSI por sus siglas en inglés).
Así también, en 2020 la agencia europea de medicamentos autorizó el uso del antibiótico de reserva Cefiderocol (Fetcroja), del grupo de las cefalosporinas, para el tratamiento de infecciones producidas por gérmenes aerobios gramnegativos, únicamente cuando existen opciones limitadas de tratamiento.
Podría mencionarse otro, la fidaxomicina, utilizada para un tipo particular de gastroenteritis producida por la bacteria Clostridium perfringens, solo cuando existe resistencia comprobada a los antibióticos tradicionales: el metronidazol y la vancomicina orales.
Esto parecería dar impulsos nuevos a la ofensiva, pero el problema está en que al ser estos ejemplos antibióticos de reserva, el uso de los mismos se encuentra aún muy limitado, lo cual impide su fabricación en lotes importantes, que a su vez significa un riesgo importante para las farmacéuticas encargadas de la producción y distribución de estos.
Alianzas público-privadas
Se han sugerido iniciativas privadas, con el apoyo de los gobiernos, para hacer frente a este acuciante problema. Tras el azote de una pandemia como el coronavirus, se han visto dinámicas muy interesantes.
En este aspecto, el director general de la compañía suiza BioVersys, el Dr. Marc Gitzinger, propone un nuevo modelo de negocio en el cual no se generen pérdidas durante el desarrollo e implementación de nuevos antibióticos. La iniciativa BEAM (Biotech companies from Europe innovating in AntiMicrobial resistance research) aglutina a otras 60 compañías cuya misión consiste en generar incentivos para la inversión en esta área.
Como se puede ver, la ciencia a través de la tecnología —en este caso, la generación de antibióticos— ha contribuido a la generación de nuevos problemas, pero es únicamente con más ciencia como se podrá hacer frente a los nuevos desafíos.
¿Qué te pareció este artículo?
Osvaldo Meza es médico especializado en Medicina Interna por la Universidad Católica de Asunción (UCA) y editor de Ciencias Médicas en Ciencia del Sur. Forma parte de la Asociación Paraguaya Racionalista, y entre sus aficiones se encuentran la física, astronomía, la divulgación científica y el pensamiento crítico.








 (4 votos, promedio: 4,75 de 5)
(4 votos, promedio: 4,75 de 5)