“A pesar de casi cuatro décadas de esfuerzos por parte de la comunidad de investigación mundial, una vacuna eficaz para prevenir el VIH sigue siendo un objetivo difícil de alcanzar”, declaró en enero de 2022 el Dr. Anthony Fauci, director del Instituto Nacional de Alergias y Enfermedades Infecciosas (NIAID) de EE. UU.
Las vacunas de ARN mensajero (ARNm) muestran un notable éxito en el combate del SARS-CoV-2. Esto ayudó en gran medida al lanzamiento de esta tecnología al mercado. Sin embargo, a pesar de que el uso en humanos es reciente, los investigadores han estado estudiando la tecnología de ARNm para otros usos durante décadas. Ahora, uno de los grandes desafíos es desarrollar una vacuna contra el hasta ahora escurridizo virus de la inmunodeficiencia humana (VIH).
Una vez en el cuerpo, el ARNm contenido en las vacunas ingresa a las células y les indica a estas que produzcan ciertas proteínas que pertenecen a un virus u otro microorganismo. Estas proteínas, que son inofensivas, pueden estimular la respuesta inmune del cuerpo. En esa respuesta inmunitaria se producen anticuerpos y se activan algunas células que ayudan a proteger al individuo contra la infección si el virus real ingresa al cuerpo.
En diciembre de 2021 fueron publicados en Nature resultados preliminares del desarrollo y prueba de una vacuna de ARNm contra el VIH en animales. El equipo de trabajo es dirigido por el Dr. Paolo Lusso del NIAID.
Cómo funciona la nueva vacuna
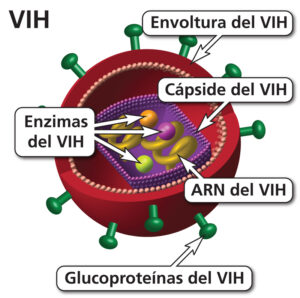
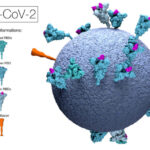
Los investigadores encapsularon el ARNm en una partícula lipídica muy pequeña que codifica dos proteínas importantes del VIH. Una de ellas es la glicoproteína de la cubierta del VIH (el equivalente de la proteína espiga del SARS-CoV-2) que muestra gran variabilidad antigénica (Env), junto a la multiproteína estructural (Gag), que es vital para el ensamblaje de partículas virales del VIH. El objetivo de esto era producir partículas similares a virus o virus-like proteins (VLP) in vivo que posean en su superficie Env glicosilado.
La vacuna experimental contra el VIH se inyecta en el músculo, donde da instrucciones para producir las dos proteínas, Env y Gag. Las células musculares ensamblan estas dos proteínas en VLP. Las VLP no pueden causar infección o enfermedad porque carecen del código genético completo del VIH; sin embargo, provocan respuestas inmunitarias similares a la infección natural por el VIH.
En el estudio, las VLP que poseen Env en su superficie provocaron anticuerpos ampliamente neutralizantes y otras respuestas inmunitarias que protegían contra el desafío viral en un modelo de mono. Aunque las VLP no fueron tan inmunogénicas ni tan eficaces como las vacunas de ARNm contra la COVID-19, estos resultados son alentadores.
El logro obtenido no es trivial, ya que normalmente Env no logra inducir el tipo correcto de anticuerpos, incluso en la mayoría de las personas infectadas con el VIH. Si se compara las Env con la proteína espiga del SARS-CoV-2 (que es una proteína relativamente estable y no tan compleja), Env es extremadamente compleja y variable, y, entre otras cosas, posee azúcares alrededor de ella que las protegen del reconocimiento de los anticuerpos.
En el mencionado estudio, los anticuerpos provocados por la vacuna de ARNm de Env-Gag pudieron neutralizar a 11 de 12 aislados de VIH-1, pertenecientes a un panel global de referencia de Env de diferentes orígenes genéticos y geográficos. Esto representa un gran paso adelante para una vacuna contra el VIH.
De animales a humanos
Durante el ensayo, los investigadores primero probaron la vacuna en ratones. Descubrieron que, después de dos inyecciones, la vacuna provocó anticuerpos que podían neutralizar el VIH en todos los ratones estudiados. Esto representa una mejora con respecto a las anteriores vacunas experimentales contra el VIH.
Luego, probaron la vacuna en macacos Rhesus. Todos los macacos vacunados habían desarrollado niveles medibles de anticuerpos que podían neutralizar muchas cepas diversas del VIH. La vacuna experimental también indujo otras respuestas inmunitarias importantes, como las células T auxiliares, que ayudan a otras células inmunitarias.
En general, los monos vacunados tenían un 79 % menos de riesgo de infección por SHIV (simian-human HIV) por exposición que los animales no vacunados. El curso de la vacuna fue bien tolerado con solo efectos secundarios leves. Estos resultados mostraron que la nueva vacuna contra el VIH era segura y que provocó respuestas inmunitarias contra un virus similar al VIH.
El equipo planea realizar un ensayo de Fase 1 de la vacuna de ARNm contra el VIH en voluntarios adultos sanos después de un mayor refinamiento y pruebas, ya que se necesitan 7 dosis sucesivas para lograr el nivel de inmunidad descrito, lo que sería difícil de implementar en humanos.
Las tecnologías de vacunas de ARNm han pasado por varios problemas, los cuales, luego de décadas de investigación se fueron superando. Entre algunas de las dificultades vencidas se encuentran su inestabilidad y la inmunogenicidad desfavorable. Por otro lado, las ventajas que ofrecen las vacunas de ARNm son importantes, comparadas con las plataformas tradicionales aplicadas en el campo del VIH u otras enfermedades. Entre ellas están la rapidez de desarrollo, la facilidad de fabricación y la escalabilidad.
El ARNm también es considerablemente más barato de producir y puede modificarse rápidamente según sea necesario, una consideración importante para los virus que mutan rápidamente como el VIH.
¿Qué te pareció este artículo?
Columnista y editora científica de Ciencia del Sur. MSc y PhD en Biología Parasitaria con énfasis en Biología Molecular aplicada a microorganismos por el Instituto Osvaldo Cruz (Fiocruz) de Río de Janeiro, Brasil. Fabiola obtuvo su licenciatura en Biología de la Facultad de Ciencias Naturales y Exactas de la Universidad Nacional de Asunción.
Realizó un posdoctorado en la Universidad de Bath (Inglaterra) y es colaboradora externa del Centro para el Desarrollo de la Investigación Cientifica.
Actualmente es Research Assistant en el Instituto Sanger de Cambridge, Reino Unido.